Navegação
- Autor
- Materiais de Engenharia
- Borracha
- Proj. de Artefactos
- Processos
- Referências
- Referências
- Livros Técnicos
- Artigos Técnicos
- Portugueses na Indústria da Borracha
- Abreviaturas Utilizadas na Indústria da Borracha
- Websites com Interesse
- Trabalhos do Autor
- A Minha Vida na I. B.
- Novas Publicações
- Trabalhos de Outros Autores
- Ensaios, Formação, Consultoria e Estudos de Caso
- Sugestões para Outras Áreas Industriais
- CTBorracha SP
Enxofre
O enxofre foi o primeiro agente de vulcanização conhecido. Deve-se ao americano Charles Goodyear a sua descoberta, em 1839. Como já vimos na página Vulcanização, a sua descoberta foi disputada também pelo inglês Thomas Hancock. Existem diversas variedades de enxofre para borracha. O enxofre pode apresentar-se na forma:
- De pó, com diferente granulometria (por exemplo, 120 a 300 mesh);
- De pó revestido com óleo (por exemplo, com 1,0%, 2,5% ou 5,0% de óleo);
- De pó, em combinação com agentes dispersantes orgânicos ou inorgânicos;
- Granulada, pré-dispersa em borracha e agentes dispersantes.
A dispersão do enxofre nalguns tipos de borracha é difícil (por exemplo, na borracha de acrilonitrilo butadieno, borracha de etileno propileno dieno e em borracha butílica). Nestes casos, é recomendada a utilização de enxofre nas formas 3 ou 4.
Por outro lado, a solubilidade do enxofre nos diversos tipos de borracha é muito diversa. Bastante mais solúvel nas borrachas natural (NR) e de estireno butadieno (SBR) do que na borracha de polibutadieno (BR), é vulgar surgirem problemas em misturas de NR/BR ou de SBR/BR porque, sendo a migração do enxofre muito mais rápida na borracha de polibutadieno, longos períodos de armazenagem podem dar lugar à formação de cristais de enxofre na fase da borracha de polibutadieno e ocorrer uma sensível perda de propriedades no vulcanizado se não forem tomadas medidas correctivas, como, por exemplo, uma cuidada remistura do composto antes da sua utilização.
No Quadro 1 apresenta-se a solubilidade do enxofre em vários tipos de borrachas, a diferentes temperaturas.
| Quadro 1 – Solubilidade do enxofre em vários tipos de borracha, a diferentes temperaturas (% em peso) |
||||||||
|---|---|---|---|---|---|---|---|---|
| Temp. ºC | NR | SBR | OE-SBR | BR | CR | NBR | IIR | EPR |
| 20 | 1,3 | 1,2 | 1,5 | 1,0 | – | 0,3 | – | – |
| 25 | 1,4 | – | – | – | – | – | – | 0,3 |
| 40 | 2,1 | 1,6 | 1,7 | 1,5 | – | 0,5 | 0,06 | – |
| 50 | 3,2 | 3,4 | – | – | 3,4 | 1,1 | 0,8 | – |
| 80 | 5,6 | 6,1 | – | – | – | 2,1 | 1,7 | – |
| 93 | 7,1 | 8,8 | – | – | – | – | – | 2,6 |
| 120 | 10,2 | – | – | – | – | – | – | – |
| Nota:
Fonte: “Elastomer Processing – Formulas and Tables”, Kleemann/Weber, Hanser Verlag, Munich, 1998, pág. 49. |
||||||||
O enxofre apresenta mais de 30 formas alotrópicas. Das diferentes formas alotrópicas de enxofre, as mais vulgares são constituídas por anéis com 8 átomos (S8): Sα, Sβ e Sγ. Destas, a variedade mais estável é Sα, bastante estável até 95ºC e que cristaliza no sistema ortorrômbico; a 95,5ºC, a variedade Sα transforma-se em Sβ, reacção que é acompanhada de aumento de volume; esta variedade alotrópica cristaliza no sistema monoclínico e é estável até 119,7ºC, temperatura em que ocorre a fusão. A variedade Sγ cristaliza no sistema monoclínico e, como é instável a todas as temperaturas, apresenta tendência para reverter para a variedade alotrópica ortorrômbica Sα.
Estas variedades cristalinas de enxofre podem distinguir-se, para além do sistema de cristalização, pela sua cor e pela sua densidade. Assim, o enxofre Sα apresenta-se em cristais ortorrômbicos, de cor amarelo esverdeado e tem a densidade 2,07; o enxofre Sβ apresenta-se em cristais monoclínicos, de forma acicular, de cor amarelo âmbar, e tem a densidade 1,96; o enxofre Sγ apresenta-se em cristais monoclínicos em forma de agulhas, de cor amarelo pálido e tem a densidade de 1,92.
Existem também variedades alotrópicas constituídas por anéis com 7 e com 6 átomos de enxofre. Os anéis com 7 átomos de enxofre apresentam 4 variedades conhecidas: S7 α, β, γ e δ. Os anéis S7 possuem uma cor amarelo- brilhante. Os anéis com 6 átomos de enxofre S6 apresentam a forma de uma cadeira (Figura 1).
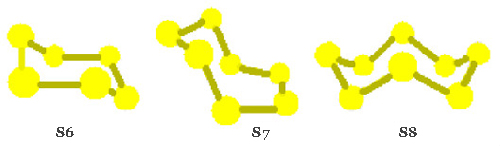 Figura 1 – Disposição espacial de anéis de enxofre com 6, 7 e 8 átomos
Figura 1 – Disposição espacial de anéis de enxofre com 6, 7 e 8 átomosExistem ainda muitas outras variedades alotrópicas, com 2 e 3 átomos de enxofre (em formas gasosas de enxofre) e em formas sólidas, com 10, 15, 18 e 20 átomos de enxofre. Todas as variedades referidas são solúveis em sulfureto de carbono.
A variante que é utilizada na Indústria da Borracha é o enxofre Sα, devidamente micronizado e nas formas que atrás referimos.
Processos de obtenção do enxofre
O enxofre existe na natureza no estado nativo (Figura 2), em minérios metálicos, sob a forma de sulfuretos, no carvão e nos produtos petrolíferos (gás natural ou crude).
 Fig. 2 – Cristal de enxofre embebido
Fig. 2 – Cristal de enxofre embebidonuma matriz de cristais de calcite
O enxofre que existe no estado nativo, pode ser extraído por actividade mineira tradicional ou pelo método de Frash, método inventado em 1894 pelo americano, de origem alemã, Herman Frash.
O enxofre que existe sob a forma de sulfuretos metálicos, pode ser obtido mediante a grelhagem dos minérios (pirites, por exemplo), e depois por redução de SO2 ou pelo processo Claus (processo inventado pelo inglês C.F. Claus e patenteado em 1883):
3 O2 + 2 H2S → 2 SO2 + 2 H2O
SO2 + 2 H2S → 3 S + 2 H2O
O enxofre pode ser também obtido, via gaseificação do carvão, pelo mesmo processo Claus, atrás referido.
Finalmente, o enxofre pode ser obtido dos produtos de origem petrolífera, seja no gás natural seja no próprio crude.
O enxofre presente no gás natural apresenta-se sob a forma de ácido sulfídrico (H2S); todos os tipos de gás que contenham ácido sulfídrico em quantidades superiores a 5,7 mg/m3 são designados por sour gas. O enxofre é obtido, por tratamento do gás, pelo processo Claus.
No caso do crude, a extracção do enxofre é um pouco mais complexa. O sour crude oil (crude contendo mais do 0,5% de enxofre) é tratado num reactor com hidrogénio, a uma temperatura de 300-380ºC, na presença de um catalisador, o qual promove, entre outras reacções, a hidrogenação do enxofre, com formação de H2S. A separação do ácido sulfídrico é efectuada a seguir, fazendo borbulhar a corrente de hidrocarbonetos numa solução aquosa de dietanolamina (DEA), sob pressão; nestas condições, o ácido sulfídrico dissolve-se na dietanolamina. O ácido sulfídrico dissolvido na solução aquosa de dietanolamina é depois separado por aquecimento a baixa pressão e a corrente gasosa sulfídrica é posteriormente convertida em enxofre pelo processo Claus.

